
敬畏生命,为爱发声
微信扫一扫 →
加客服免费咨询


敬畏生命,为爱发声
微信扫一扫 →
加客服免费咨询

发布时间:2025-09-26 文章编辑:药队长 推荐人数:
康奈非尼(Braftovi)是一种针对BRAF基因突变的靶向治疗药物,主要用于治疗BRAF-V600E或V600K突变阳性的不可切除或转移性黑色素tumor以及BRAF-V600E突变阳性的转移性CRC。由于其特定的作用机制,康奈非尼在治疗这些类型的CA中发挥着重要的作用。
在使用康奈非尼之前,首先需要进行患者选择,确保药物能够针对具有特定BRAF基因突变的tumor。
(1)BRAF-V600E或V600K突变阳性不可切除或转移性黑色素tumor:在开始使用康奈非尼之前,必须确认患者的tumor标本中存在BRAF-V600E或V600K突变。
(2)BRAF-V600E突变阳性转移性CRC:同样,在开始使用康奈非尼之前,必须确认患者的tumor标本中存在BRAF-V600E突变。

对于此类患者,康奈非尼的推荐剂量为450mg(即6粒75mg胶囊),每日一次。康奈非尼需要与比美替尼联合使用,直至疾病进展或出现不可接受的毒性。关于比美替尼的推荐剂量信息,请参考比美替尼的处方信息。
对于此类患者,康奈非尼的推荐剂量为300mg(即4粒75mg胶囊),每日一次。康奈非尼需要与西妥昔单抗联合使用,直至疾病进展或出现不可接受的毒性。关于西妥昔单抗的推荐剂量信息,请参考西妥昔单抗的处方信息。
(1)康奈非尼可以与食物一起服用,也可以不与食物一起服用。但是,请确保不要在下一剂后12小时内服用遗漏的剂量。如果忘记服用康奈非尼,请继续按照规定的剂量和时间表服用下一剂,不要额外补充遗漏的剂量。
(2)如果在服用康奈非尼后出现呕吐,请不要再额外补充服用剂量,而是继续按照规定的剂量和时间表等待服用下一个剂量。
如果停用比美替尼,将康奈非尼的最大剂量减少至300mg(4粒75g胶囊),每天一次,直到比美替尼恢复使用,与康奈非尼相关的不良反应的剂量减少见表1。
表1.针对康奈非尼治疗黑色素tumor出现的不良反应的推荐剂量调整

如果停用西妥昔单抗,则停用康奈非尼,与康奈非尼相关不良反应的剂量减少如表2所示。
表2.针对康奈非尼治疗CRC出现的不良反应的推荐剂量调整

表3:针对康奈非尼不良反应的建议剂量调整
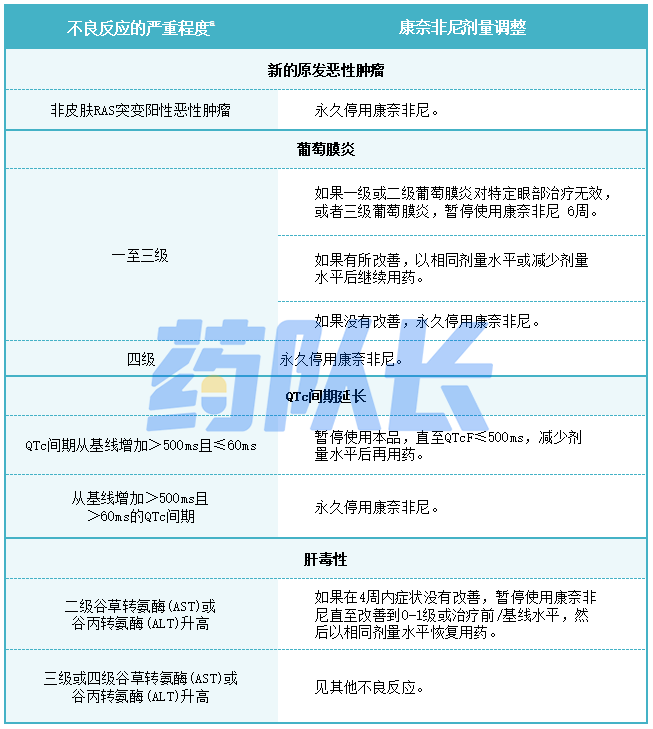
a:美国国家CA研究所CTCAEV4.03版。
b:对于新的原发性皮肤恶性tumor,除葡萄膜炎、虹膜炎和虹膜睡状体炎以外的眼部事件,以及间质性肺病/肺炎、心脏功能障碍、肌酸磷酸激酶CPK升高、横纹肌溶解症和静脉血栓栓塞以外,不建议在与比美替尼或西妥昔单抗联合用药时调整康奈非尼的剂量。
参考比美替尼或西妥昔单抗处方信息,出现每种产品相关的不良反应时,需要遵医嘱调整剂量。了解更多康奈非尼信息,点击免费在线咨询
应避免康奈非尼与强或中度CYP3A4抑制剂联合给药,如果无法避免联合用药,根据表4中的建议减少康奈非尼的剂量,并且在CYP3A4抑制剂停药3-5个消除半衰期后,重新恢复CYP3A4抑制剂用药前康奈非尼的用量。
表4:康奈非尼与强或中度CYP3A4抑制剂合用时的剂量调整
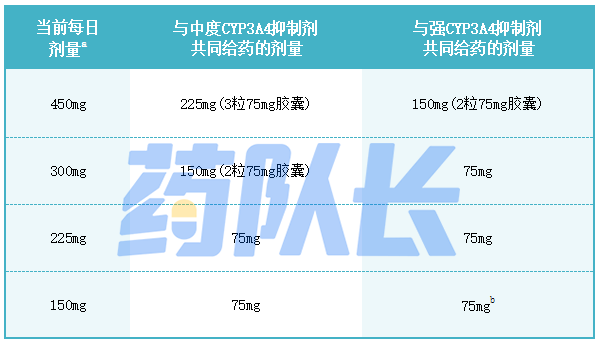
a:当前日剂量是指根据适应症推荐的康奈非尼剂量,或根据表1(黑色素tumor)和表2(CRC)中针对不良反应制定的剂量。
b:康奈非尼与强CYP3A4抑制剂联合给药时,使用75mg康奈非尼剂量的暴露量,预计高于不与CYP3A4抑制剂联合用药下150mg剂量的康奈非尼暴露量,类似于不与CYP3A4抑制剂联合使用下225mg康奈非尼的暴露量。用药时要密切监测患者的不良反应,在使用150mg剂量水平的康奈非尼时,若需要和强或中度CYP3A4抑制剂联用,应由专业医生进行临床判断。
免责声明:本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
参考资料:FDA说明书,FDA更新于2024年12月的说明书https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=210496
康奈非尼(Encorafenib)作为BRAF激酶抑制剂,与比美替尼联合用于治疗BRAFV600E或V...【详情】
推荐指数:1092025-10-27
康奈非尼(Braftovi)是一种激酶抑制剂,能够抑制编码B-raf蛋白的BRAF基因,从而减...【详情】
推荐指数:2132025-09-26
康奈非尼是一种用于治疗特定基因突变的靶向药物,主要用于黑色素病变和结...【详情】
推荐指数:1832025-09-26
康奈非尼(Encorafenib)是一种用于治疗BRAF-V600E或V600K突变阳性不可切除或转移...【详情】
推荐指数:1412025-09-26
康奈非尼(Braftovi)作为一种新型的靶向治疗药物,在针对具有BRAF V600E或V60...【详情】
推荐指数:2492025-09-26
康奈非尼(Braftovi)是一款靶向治疗药物,由法国Pierre Fabre公司研发。该药主要用...【详情】
推荐指数:3602025-09-26
在使用康奈非尼之前,患者应咨询医生以了解更多的细节,包括药物的使用方...【详情】
推荐指数:1742025-09-26
康奈非尼(Braftovi)是一种针对BRAF基因突变的靶向治疗药物,主要用于治疗BRAF...【详情】
推荐指数:2882025-09-26
2025年12月22日,,罗氏集团对外宣布,美国食品药品监督管理局(FDA)已正式【详情】
推荐指数:1272025-12-23
2025年12月18日,海罗赛姆治疗学公司宣布,强生公司已获得美国食品药品【详情】
推荐指数:1102025-12-19
2025年12月15日,斯普劳特制药公司今日宣布一项女性健康领域的里程碑事【详情】
推荐指数:412025-12-16
近日,赛尔群公司(Celltrion,Inc.)宣布,其参照Eylea(阿柏西普2mg)研发的生物【详情】
推荐指数:992025-12-01
2025年11月25日,美国食品药品监督管理局(FDA)批准度伐利尤单抗(商品名:【详情】
推荐指数:1402025-11-26
2025年11月20日,英塔斯制药有限公司旗下专注于肿瘤学、免疫学和危重症【详情】
推荐指数:1362025-11-21
欧洲药品管理局人用药品委员会(CHMP)已推荐批准他法西他单抗(Minjuvi)联合【详情】
推荐指数:1202025-11-18
2025年10月16日,欧洲药品管理局(EMA)人用药品委员会(CHMP)通过积极意见,建【详情】
推荐指数:442025-11-13
2025年11月17日,上海复宏汉霖生物技术股份有限公司与欧加隆(Organon)宣布【详情】
推荐指数:422025-11-18
美国食品药品监督管理局(FDA)近日宣布了一项重要政策调整:取消对当前【详情】
推荐指数:362025-09-26
2025年8月6日,美国食品药品监督管理局(FDA)加速批准了dordaviprone(商品名【详情】
推荐指数:372025-09-26
2025年10月13日,BlacksmithMedicines生物制药公司宣布,美国食品药品监督管理【详情】
推荐指数:482025-09-26
生物医药公司BrightGene Bio Medical Technology (Shanghai) Co., Ltd. (勃林格殷格翰,【详情】
推荐指数:712025-09-26
美国食品药品监督管理局(FDA)近日批准生物制药公司PTC Therapeutics研发的【详情】
推荐指数:302025-09-26
2025年9月8日,创新型LIBERTY®血管内机器人系统的研发与制造商MicrobotMedi【详情】
推荐指数:362025-09-26
迪哲医药(Dizal)宣布将在2025年美国临床肿瘤学会(ASCO)年会上展示其在血液【详情】
推荐指数:472025-09-26
 鲁公网安备37010402441285号
鲁ICP备2023035557号-2
互联网药品信息服务资格证书 证书编号:(鲁)-经营性-2022-0196
鲁公网安备37010402441285号
鲁ICP备2023035557号-2
互联网药品信息服务资格证书 证书编号:(鲁)-经营性-2022-0196